真核有参转录组
产品介绍
转录调控
转录组测序(RNA-seq)是目前高通量测序技术中被用得最广的一种技术,可以帮助我们了解各种比较条件下,所有基因的表达情况的差异。它可以检测的差异有:正常组织和肿瘤组织的之间的差异;也可以检测药物治疗前后基因表达的差异;还可以检测发育过程中,不同的发育阶段,不同的组织之间的基因表达差异。诸如此类。同时还可以检测 RNA 的结构上的差异。例如可变剪接,融合基因,单核苷酸多态性(SNP)等。
应用领域
基因表达谱分析、基因调控机制、生物识别与分类、药物筛选与副作用研究、疾病的分子机制研究等。
应用介绍
生物学研究: 您可以使用快速获得感兴趣的细胞、组织或生物体内mRNA的种类及其丰度,并发现由于可变剪接或SNP的选择而产生新的mRNA isoform,同时,您也可通过分析不同细胞或不同组织中mRNA的种类及其丰度,来进一步研究mRNA的差异表达信息。通过对差异表达基因进行功能分析,可发现细胞分化过程中基因表达调控变化的整体特征,以及在机体发育,信号传递等生物学过程中的作用。如果您希望研究某种基因如何通过改变细胞基因表达调控网络来发挥其生物学功能,您可以进行突变、敲除或敲低该基因,并比较实验组和对照组的RNA-seq分析结果。通过差异表达分析,您可以快速全面地获得所需信息
医学研究: 在癌变和其他复杂疾病的发生和发展过程中,细胞内的基因表达模式会发生显著改变。如果您是临床医生或相关研究人员,希望快速全面了解您感兴趣的癌症或其他疾病发生过程中基因表达模式的变化,以为该疾病的诊断和治疗提供重要的解决方案。通过对照正常样本和疾病样本中表达模式发生显著变化的基因以及其功能分析,RNA-seq技术可以快速帮您找到正确答案。
分析流程

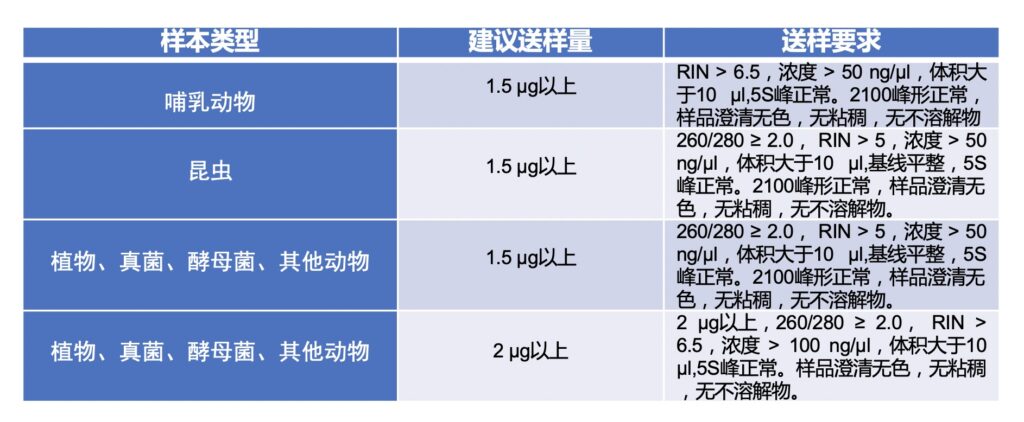
送样要求
结果展示

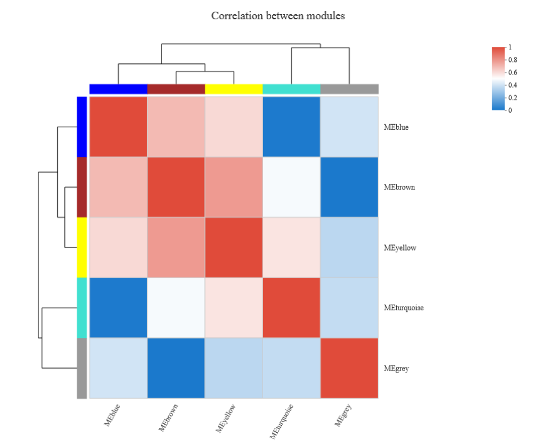
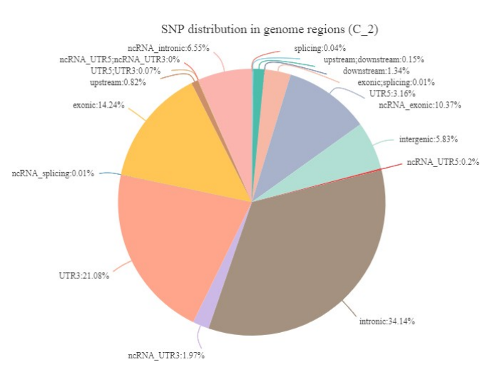
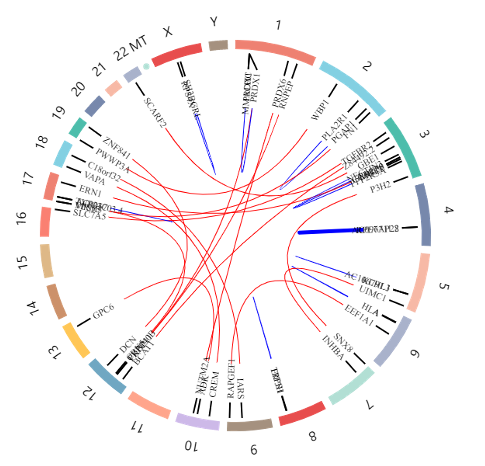


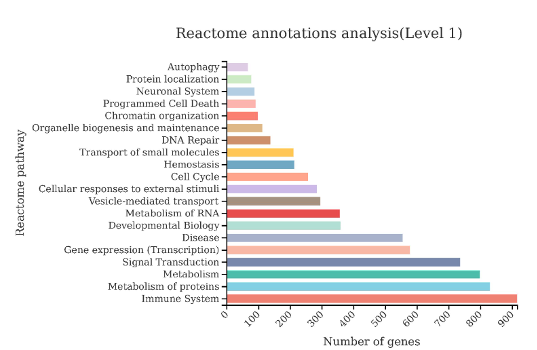
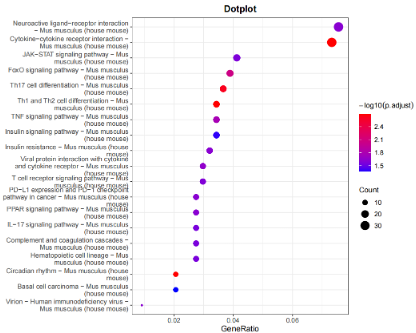
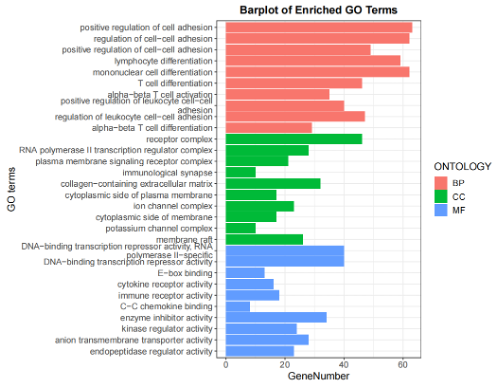
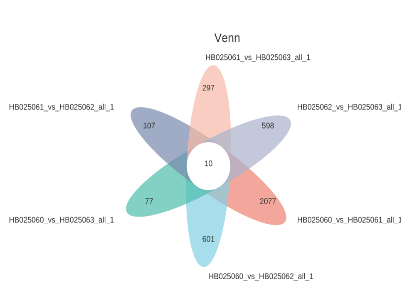
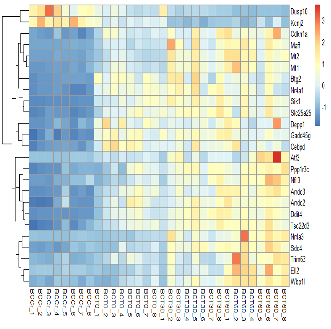
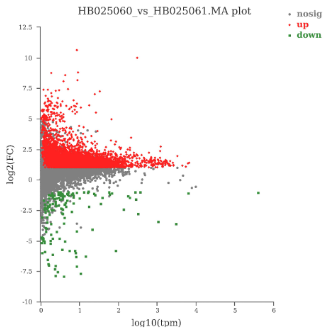
文献案例
CST1通过OTUB1调控GPX4蛋白稳定性抑制铁死亡并促进胃癌转移
CST1 inhibits ferroptosis and promotes gastric cancer metastasis by regulating GPX4 protein stability via OTUB1
期刊:Oncogene 发表时间:2023年1月 单位:苏州大学苏州医学院
研究背景
转移是导致胃癌患者预后不良的重要因素;然而,导致这种细胞行为的分子机制仍然没有得到很好的理解。胃癌腹膜转移发生率高,早期诊断困难,发生机制不明确的同时预后较差。最近的资料显示,化疗后的整体疗效和预后仍然较差。因此,寻找胃癌转移患者的新治疗方法是至关重要的
研究方法
本研究采用胃癌合并腹膜转移惠者的临床标本进行全转录组测序分析及相关分子机制研究。测序后,筛选许多lncrna和mrna进行进一步加权基因共表达网络分析(WGCNA)。通过cytoHubba鉴定gcpm相关枢纽lncrna和基因,并通过实时荧光定量PCR (qRT-PCR)、受试者工作特征曲线(ROC)分析和Kaplan-Meier生存分析验证。GO、KEGG和GSEA显示gcpm相关通路。相关分析揭示了枢纽lncrna与基因之间的潜在关系。
研究结果
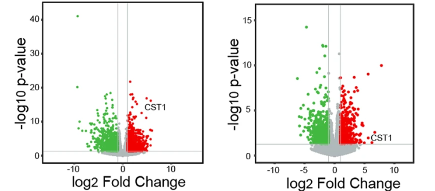
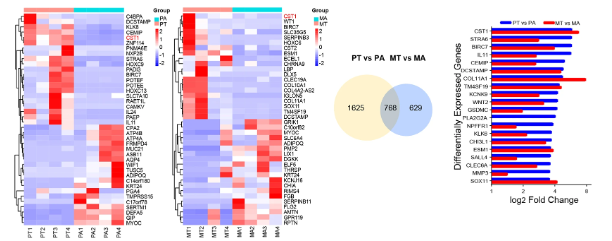
1. RNA-seq结果显示了3904个不同的基因,热图显示了最高和最低的20个表达基因。在差异表达基因中,CST1在原发性胃癌组织中显著上调。火山图显示了一致的结果。然后,我们再次对4对腹膜转移性胃癌组织进行RNA-seq分析。相应的对照、热图和火山图显示,CST1在该队列中也上调。然后,上调基因的Venn图显示了两个集群中常见和特异性基因的数量,共筛选到768个常见上调基因。CST1在胃癌和腹膜转移的胃癌组织中表达上调。
2.通过WGCNA分析联合临床样本验证,发现InC-TRIM28-14是胃癌腹膜转移潜在的诊断、预后标志物。
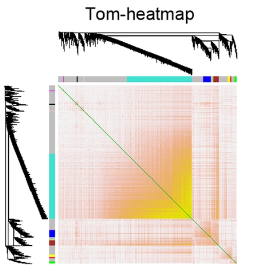
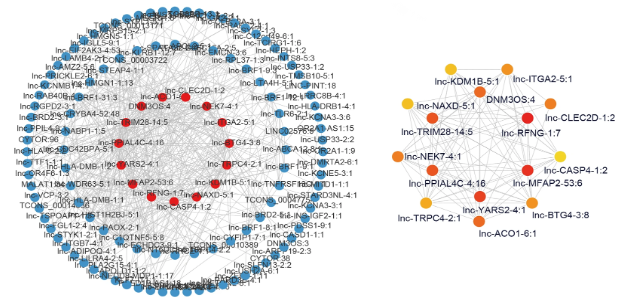
3.红色模块与腹膜转移相关(r = 0.47, p = 0.03)。可视化了红色模块100个基因的MM和GS,发现它们之间存在显著的相关性(r = 0.34, p = 0.00054)。我们使用与上述方法类似的方法,在Cytoscape中构建了500个顶边的基因共表达网络,并选择了15个程度和MCC值最高的基因。最后,六个程度最高的基因(CD93、COL1A2、COL3A1、COL4A1、COL4A2和COL6A1)随后被确定为GCPM的候选枢纽基因。
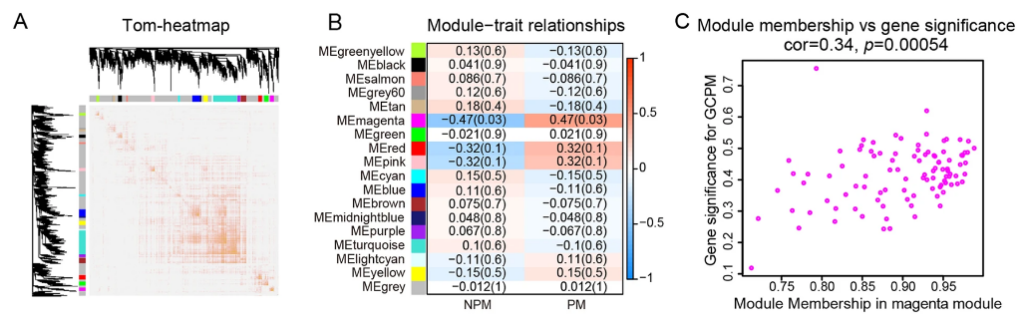
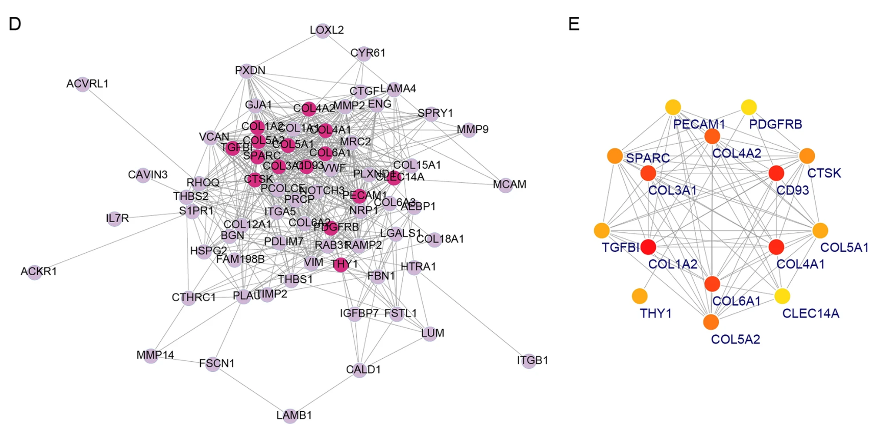
4.基于体液、组织、细胞及动物多水平的研究初步阐释了CST1、Inc-TRIM28-14、circGOSR1等分子在胃癌腹膜转移中的重要作用及关键机理,并有望成为胃癌腹膜转移临床转化应用的新的肿瘤学标志物及精准治疗靶点。
